Щавелевая кислота - это органическое соединение, которое часто используется в медицине и пищевой промышленности. Она обладает кислыми свойствами и широко применяется в качестве пищевой добавки и регулятора кислотности. Это бесцветная кристаллическая субстанция, которая хорошо растворяется в воде.
В молекуле щавелевой кислоты, химическая формула которой C4H6O6, имеется несколько типов связей между атомами. Сигма-связь - это прямая химическая связь между атомами, образующаяся при перекрытии их электронных облаков. В молекуле щавелевой кислоты существуют сигма-связи между каждым атомом углерода и взаимодействующими атомами водорода и кислорода.
Пи связь - это тип химической связи, образующейся при независимом перекрытии плоских электронных облаков атомов. В молекуле щавелевой кислоты есть пи связи между атомами углерода и кислорода, а также между атомами кислорода.
Молекула щавелевой кислоты: сколько связей?

В молекуле щавелевой кислоты можно выделить следующие типы связей:
- Одиночные (σ) связи: между углеродом (C) и каждым из двух атомов водорода (H);
- Одиночная (σ) связь: между одним из атомов углерода (C) и одним из атомов кислорода (O);
- Двойные (π) связи: между оставшимся атомом углерода (C) и каждым из двух атомов кислорода (O).
Таким образом, в молекуле щавелевой кислоты содержится 6 одиночных (σ) связей и 2 двойные (π) связи.
Одиночные (σ) связи являются более прочными и длинными, чем двойные (π) связи. Эти связи влияют на структуру и химические свойства молекулы щавелевой кислоты, определяя ее реакционную способность и способность образовывать связи с другими молекулами.
Щавелевая кислота: структура и свойства

Молекула щавелевой кислоты состоит из четырех атомов углерода, двух атомов водорода и четырех атомов кислорода. Каждый атом углерода связан с атомами кислорода двумя сигма связями, образуя две карбоксильные группы. Таким образом, в молекуле щавелевой кислоты имеется две сигма связи.
Кроме того, в молекуле щавелевой кислоты есть две пи связи, образованные плисси-реакцией между атмами углерода и кислорода. Пи связи являются несимметричными и пространственно ориентированными.
Важно отметить, что щавелевая кислота является одним из простейших карбоновых кислот и используется в различных областях, включая органическую химию, пищевую промышленность и медицину.
Какие связи встречаются в молекуле щавелевой кислоты?

Молекула щавелевой кислоты (C4H6O6) содержит различные типы связей, достаточно распространенных в органической химии.
- Сигма-связи: данная молекула содержит 18 сигма-связей, т.е. типичных однозначных химических связей между атомами. Эти связи формируются путем обмена электронами и образуют основу для структуры молекулы.
- Пи-связи: в молекуле щавелевой кислоты также присутствуют несколько пи-связей. Пи-связи формируются через попарное перекрытие плоских орбиталей, образуя области электронной плотности над и под плоскостью атомов.
- Двойные и тройные связи: молекула щавелевой кислоты содержит две двойные связи, которые обеспечивают структурную устойчивость и участвуют в реакциях с другими соединениями. Также в молекуле присутствует одна тройная связь.
В целом, связи в молекуле щавелевой кислоты образуют сложную трехмерную структуру, которая определяет ее химические и физические свойства.
Значение электронной формулы для определения связей

В молекуле щавелевой кислоты (C4H4O6) есть 10 сигма связей и 6 пи связей. Электронная формула этой молекулы представляет собой графическое изображение атомов и их связей, где каждая линия представляет одну сигма связь, а каждое плоское ограниченное облако представляет одну пи связь.
Значение электронной формулы состоит в том, что она позволяет определить тип и количество связей в молекуле. Это важно для понимания химических свойств и реакций молекулы, а также для изучения ее структуры и свойств.
Электронная формула щавелевой кислоты является одним из инструментов, использование которого позволяет получить информацию о связях в молекуле и расшифровать ее химическую структуру.
Сигма связи в молекуле щавелевой кислоты

При анализе структуры щавелевой кислоты, можно установить наличие 12 сигма связей. Так как молекула содержит 4 атома углерода, каждый из которых образует 3 связи, и 6 атомов кислорода, образующих 1 связь каждый.
Сигма связи в молекуле щавелевой кислоты имеют характер спайных орбиталей, что позволяет атомам в молекуле образовывать стабильные химические связи.
Анализ структуры и типов связей в молекуле щавелевой кислоты важен для понимания ее физических и химических свойств, а также для разработки новых методов синтеза и применения в различных областях науки и технологий.
Пи связи в молекуле щавелевой кислоты
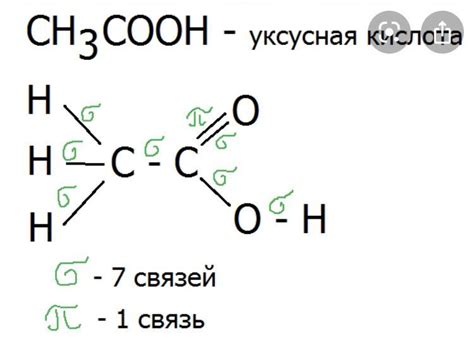
В молекуле щавелевой кислоты имеются две пи связи, которые образуются между атомами углерода и кислорода. Эти пи связи образуются вследствие наличия двойных связей между некоторыми атомами углерода и кислорода.
Пи связи обладают специфическими свойствами, включая возможность переключения электронных зарядов и участие в реакциях аддиции и аниона. Они также могут быть донорами или акцепторами электронов в реакциях обмена и позволяют молекуле обладать дополнительной структуризацией и стабильностью.
Пи связи в молекуле щавелевой кислоты играют важную роль в ее свойствах и реактивности. Они могут влиять на ее способность взаимодействовать с другими молекулами и участвовать в химических реакциях, что оказывает влияние на ее физические и химические свойства.
Количество сигма связей в молекуле щавелевой кислоты
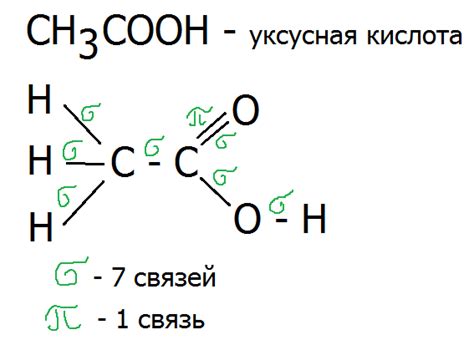
Молекула щавелевой кислоты (C4H6O6) состоит из атомов углерода (C), водорода (H) и кислорода (O). В данной молекуле нас интересует количество сигма связей, то есть связей, образованных при наложении однопорядковых электронных облаков атомов.
Чтобы определить количество сигма связей в молекуле, необходимо посчитать количество одиночных и двойных связей. В молекуле щавелевой кислоты имеются две одиночные и две двойные связи.
Таким образом, общее количество сигма связей в молекуле щавелевой кислоты равно 4.
Количество пи связей в молекуле щавелевой кислоты
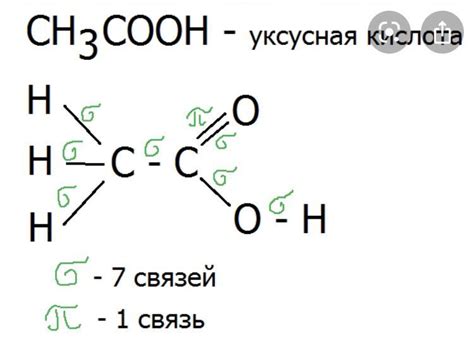
Молекула щавелевой кислоты состоит из 4 атомов углерода, 6 атомов водорода и 6 атомов кислорода. В данной молекуле имеются две π-связи. Одна из них находится между двумя атомами углерода внутри карбоксильной группы (-COOH), а другая пи связь образуется между двумя атомами углерода внутри карбонильной группы (=C=O).
Пи связи являются более слабыми по сравнению со сигма (σ) связями, но они придают молекуле щавелевой кислоты определенные свойства и химическую активность. Они существенно влияют на структуру и физические свойства этой молекулы.
